domingo, 2 de septiembre de 2018
Semana28
En esta semana yo participe mucho con mi compañera sonia en el decoracion del colegio para la antioqueñidad




Semana26
Reacciones quimicas organicas:
en las reacciones organicas generalmente ocurren dos o mas etapas en las cuales se forman unas sustancias intermedias entre los negativos y el producto final
sustrato:es la sustancia que sera atacada por el reactivo y hace parte de el producto principal
reactivo:en la qimica organica generalmete hay 3 tipos de reactivos que son:
°electrofilos
°nucleofilos
radicales libres
clasificacion de reacciones organicas:
se clasifican en polares y apolares
polares:
°reacciones de sustitucion o desplazamiento
°reaccion de adicion
°reaccioreanes de eliminacion
°reacciones de reagrupacion
°reacciones de oxidacion
°reacciones de acido-base
no polares:
°reacciones de sustitucion o desplazamiento
°reacciones de adicion
°reacciones de eliminacion
°reacciones de reagrupacion

Semana25
Reacciones organicas
son reacciones químicas que involucran al menos un compuesto orgánico como reactivo. Los tipos básicos de reacciones químicas orgánicas son reacciones de adición, reacciones de eliminación, reacciones de sustitución, y reacciones redox orgánicas. En síntesis orgánica, se usan reacciones orgánicas en la construcción de nuevas moléculas orgánicas. La producción de muchos químicos hechos por el hombre, tales como drogas, plásticos, aditivos alimentarios, textiles, dependen de las reacciones orgánicas.
laboratorio:
tema: Reconocimientos de algunos grupos funcionales y propiedades fiicas de compuestos organicos
logros:
°reconocer experimentalmente aldehidos y cetonas, accidos carboxilicos y obtener acetileno
°reconocer las porpiedades fisicas de algunos compuestos organicos
Urea:
Naftalina:

Acetato de plomo:
Acido citrico:
Acido benzoico:
Formol:
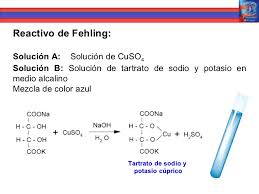



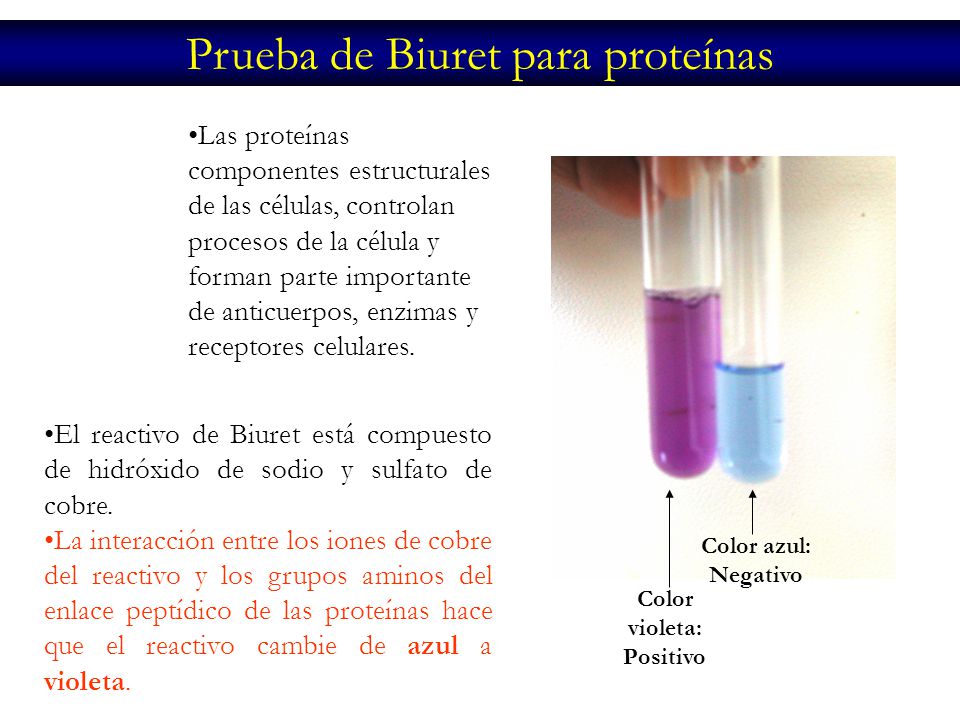
son reacciones químicas que involucran al menos un compuesto orgánico como reactivo. Los tipos básicos de reacciones químicas orgánicas son reacciones de adición, reacciones de eliminación, reacciones de sustitución, y reacciones redox orgánicas. En síntesis orgánica, se usan reacciones orgánicas en la construcción de nuevas moléculas orgánicas. La producción de muchos químicos hechos por el hombre, tales como drogas, plásticos, aditivos alimentarios, textiles, dependen de las reacciones orgánicas.
laboratorio:
tema: Reconocimientos de algunos grupos funcionales y propiedades fiicas de compuestos organicos
logros:
°reconocer experimentalmente aldehidos y cetonas, accidos carboxilicos y obtener acetileno
°reconocer las porpiedades fisicas de algunos compuestos organicos
Urea:

Naftalina:

Acetato de plomo:
Acido citrico:

Acido benzoico:

Formol:






Semana24
La proyección de Fischer
Proyectar consiste en dibujar en dos dimensiones (plano) una molécula. En la proyección de Fischer la molécula se dibuja en forma de cruz con los sustituyentes que van al fondo del plano en la vertical y los grupos que salen hacia nosotros en la horizontal, el punto intersección de ambas líneas representa el carbono proyectado.
Aunque se acostumbra a dejar la cadena carbonada en la vertical, puede girarse la molécula de diferentes formas dando lugar a proyecciones de Fischer aparentemente diferentes, pero que en realidad representan la misma molécula.
Para comprobar que la proyección está bien hecha, vamos a dar notación R/S a la molécula y a su proyección.

Para comprobar que la proyección está bien hecha, vamos a dar notación R/S a la molécula y a su proyección.
Ahora haremos la proyección de una molécula con dos centros quirales

Para proyectar una molécula en Fischer es necesario dibujarla en la conformación eclipasada. Los sustituyentes que nos quedan en el plano van colocados arriba y abajo en la proyección. Los grupos que salen hacia nosotros (cuñas) se disponen a la derecha en la proyección, y los que van al fondo (lineas a trazos) se disponen a la izquierda.
Para proyectar una molécula en Fischer es necesario dibujarla en la conformación eclipasada. Los sustituyentes que nos quedan en el plano van colocados arriba y abajo en la proyección. Los grupos que salen hacia nosotros (cuñas) se disponen a la derecha en la proyección, y los que van al fondo (lineas a trazos) se disponen a la izquierda.
Semana22
Isomeria conformacional:
En química orgánica, los isómeros conformacionales o confórmeros son estereoisómeros
que se caracterizan por poder interconvertirse (modificar su orientación espacial, convirtiéndose en otro isómero de la misma molécula) a temperatura ambiente, por rotación en torno a enlaces simples. Estas conformaciones se denominan: anti, eclipsada o alternada. Son compuestos que, generalmente, no pueden aislarse físicamente, debido a su facilidad de interconversión
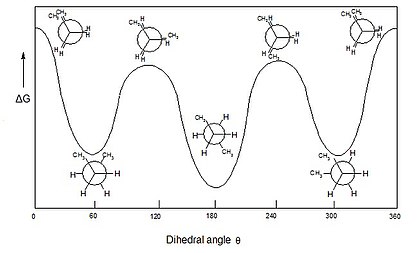
quiz sobre estructura de función, cadena y posición
En química orgánica, los isómeros conformacionales o confórmeros son estereoisómeros
que se caracterizan por poder interconvertirse (modificar su orientación espacial, convirtiéndose en otro isómero de la misma molécula) a temperatura ambiente, por rotación en torno a enlaces simples. Estas conformaciones se denominan: anti, eclipsada o alternada. Son compuestos que, generalmente, no pueden aislarse físicamente, debido a su facilidad de interconversión

quiz sobre estructura de función, cadena y posición
Semana21
Isomeria estructural:
es una forma de isomeria en la que las moléculas con la misma fórmula molecular tienen diferentes patrones de unión y organización atómica, en oposición a estereoisomerismo , en el que los enlaces moleculares están siempre en el mismo orden y solo el arreglo espacial difiere. Hay sinónimos múltiples para isómeros constitucionales.Tres categorías de isómeros constitucionales son los isómeros esqueléticos, posicionales y funcionales. Los isómeros posicionales también se llaman regioisómeros.
isomeria de cadena:
Se llaman isómeros a aquellas moléculas que poseen la misma fórmula molecular pero diferenteestructura. Se clasifican en isómeros estructurales y estereoisómeros. Los isómeros estructurales difieren en la forma de unir los átomos y a su vez se clasifican en isómeros de cadena de posición y de función
Isomería de posición:
Por ejemplo, la fórmula molecular C4H10O puede corresponder a dos sustancias isómeras que se diferencian en la posición del grupo OH: el 1-butanol y el 2-butanol.
| CH3-CH2-CH2-CH2OH | CH3-CH2-CHOH-CH3 |
|---|---|
| 1-butanol, Butan-1-ol o n-butanol | 2-butanol, Butan-2-ol o sec-butanol |
 | 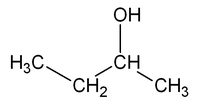 |
Este tipo de isomería resulta de la posibilidad de colocar grupos funcionales, cadenas laterales en posiciones estructuralmente no equivalentes. Supongamos que sustituimos uno de los átomos de hidrógeno del butano, CH3-CH2-CH2-CH3, por un grupo hidroxilo. Numerando los carbonos de la cadena del butano y realizando esta sustitución en el carbono extremo (C1), obtenemos un alcohol llamado butan-1-ol (1-butanol). Si sustituimos un hidrógeno del C2 por el grupo -OH, obtenemos el alcohol isómero butan-2-ol (2-butanol), que difiere en la posición del grupo hidroxilo. Obsérvese que, sin embargo, si realizamos la sustitución en el C3, no obtenemos un tercer isómero, sino de nuevo el 2-butanol. Las dos representaciones que se indican para el 2-butanol son estructuralmente idénticas, como se puede ver girando su estructura 180º alrededor de un eje.
Isomería funcional:
Por ejemplo el C3H6O puede corresponder a la molécula de propanal (función aldehído) o a la propanona (función cetona).
| CH3-CH2-CHO | CH3-CO-CH3. | |
|---|---|---|
| Propanal (función aldehído) | Propanona (función cetona) |
Esta isomería la presentan ciertos grupos de compuestos relacionados como: los alcoholes y éteres, los ácidos y ésteres, y también los aldehídos y cetonas.
Tautomería:
Artículo principal: Tautómero
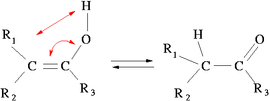
Es un tipo especial de isomería en la que existe transposición de un átomo entre las dos estructuras, generalmente hidrógeno, existiendo además un fácil equilibrio entre ambas formas tautómeras.Un ejemplo de la misma es la tautomería ceto-enólica en la que existe equilibrio entre un compuesto con grupo OH unido a uno de los átomos de carbono de un doble enlace C=C, y un compuesto con el grupo carbonilo intermedio, C=O típico de las cetonas, con transposición de un átomo de hidrógeno.
 |
|---|
Tautomería ceto-enólica. |
isomeria espacial:
moleculares idénticas y sus átomos presentan la misma distribución (la misma forma de la cadena; los mismos grupos funcionales y sustituyentes; situados en la misma posición), pero su disposición en el espacio es distinta. Los isómeros tienen igual forma en el plano. Es necesario representarlos en el espacio para visualizar las diferencias. Puede ser de dos tipos: isomería conformacional e isomería configuracional, según que los isómeros se puedan convertir uno en otro por simple rotación de enlaces simples, o no.
Semana20

Isomeria:
Compuestos organicos:
°son muy abundantes
°la mayoria poseen enlaces covalentes
°la mayoria son solubles e insolubles en h2O
°son de origen vegetal o animal
°la mayoria son combustibles

Compuestos inorganicos:
-hay muy pocos
-la mayoria poseen enlaces tonicos
-la mayoria son solubles en H2O e insolubles en organicos
-la mayorria no son combustibles

Suscribirse a:
Comentarios (Atom)










